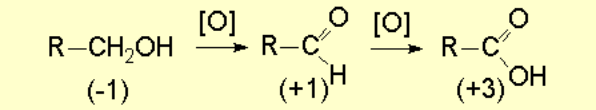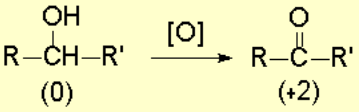Los alcoholes pueden obtenerse por reducción de otras funciones más oxidadas. Es fácil imaginar lo contario.
En un alcohol primario, el carbono que soporta el grupo OH tiene un estado de oxidación formal -1 por lo que aún tiene múltiples posibilidades de oxidación.
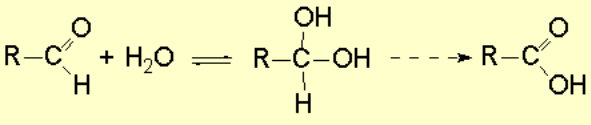
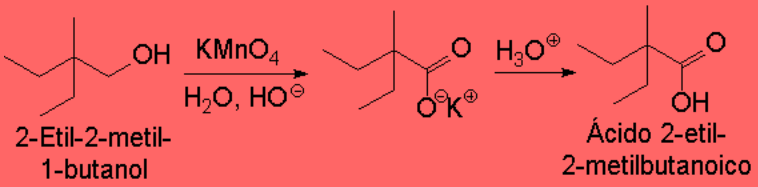
Muchos reactivos de oxidación son sales inorgánicas, como KMnO4, K2Cr2O7, sólo solubles en agua. El agua produce hidratos con los aldehídos, provocando que la oxidación de la 2ª etapa (aldehídos a ácidos carboxílicos) sea más fácil que la 1ª.
Es difícil pararse en el aldehído.
Para lograrlo hay que utilizar reactivos que tengan una parte orgánica, solubles en disolventes orgánicos, para evitar la presencia de agua.
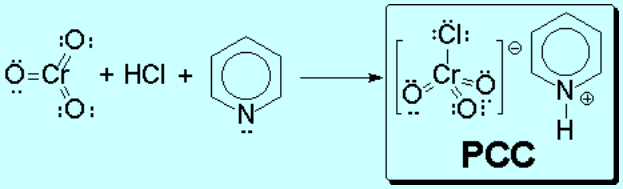
Clorocromato de piridinio
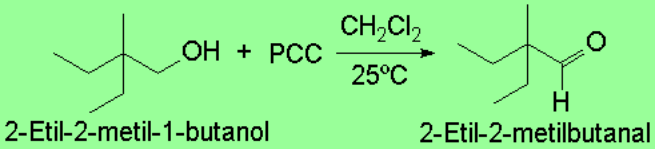
PCC
El PCC es soluble en disolventes orgánicos. Su reacción con alcoholes primarios es selectiva y se detiene en el aldehído.
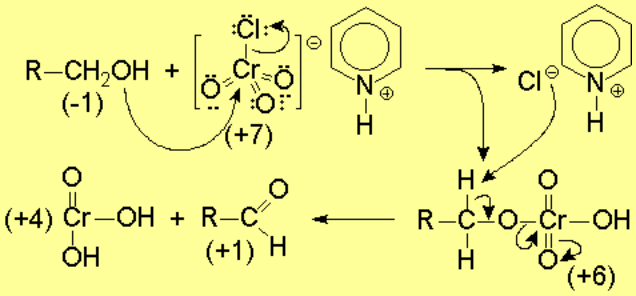
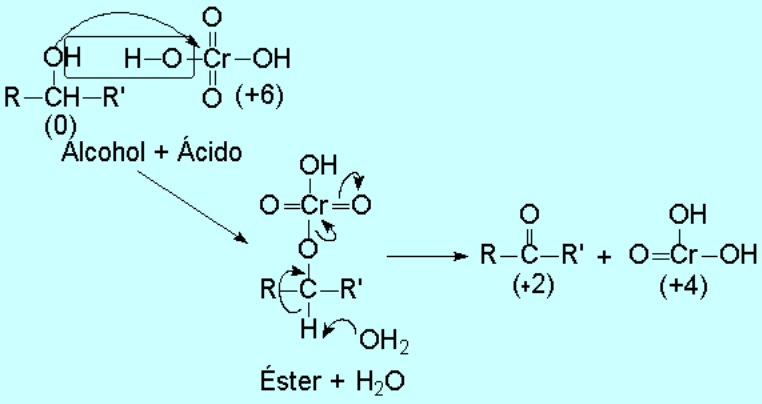
Un mecanismo posible para esta reacción es:
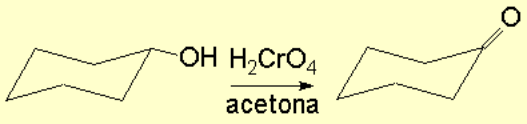
Se pueden transformar en cetonas, sin que la molécula se rompa, lo que podría suceder si se fuerzan las condiciones de reacción
Un mecanismo posible para esta reacción es:
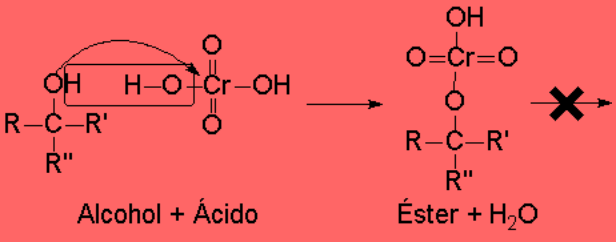
Los alcoholes terciarios no pueden dar esta reacción porque carecen de un hidrógeno que poder eliminar.
Son muy resistentes a la oxidación