
J.J. Thomson
Determinó la relación
carga/masa del electrón en 1897.
|
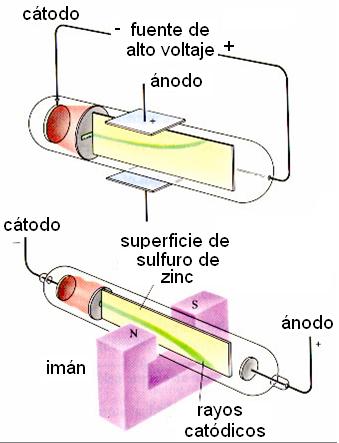
Un conjunto de partículas que poseen masa y carga se desvían
en presencia de un campo eléctrico o magnético. Al aplicar
una diferencia de voltaje muy elevado entre dos placas metálicas,
los átomos de los metales de la placa negativa pierden los electrones
que vuelan en el vacío hacia la placa cargada positivamente. Si en
el camino de vuelo existe una diferencia de voltaje entre otras dos placas
(figura superior) o un campo magnético generado por un imán
potente (figura inferior), los electrones se desvían, lo que prueba
que tienen masa y carga.
|
En los extremos de una
ampolla de vidrio, en la que se ha hecho el vacío, se sitúan
dos placas metálicas (electrodos, cátodo y ánodo)
. Si entre ellas se crea una diferencia de voltaje eléctrico suficientemente
elevada, se produce una descarga. Si disponemos a lo largo del eje de la
descarga una superficie de sulfuro de zinc, veremos que la superficie muestra
un rayo luminoso (rayos catódicos). Este rayo está formado
por partículas de carga negativa porque en presencia de un campo
eléctrico, el rayo se desvía hacia el polo positivo (ánodo
en la figura superior). Las partículas son los electrones que poseen
una cierta masa y una carga negativa. Aplicando campos eléctricos
y magnáticos a los rayor catódicos, Thomson fue capaz de
medir la relación masa/carga del electrón.
|
